La traduction
Fondamental : Le code génétique
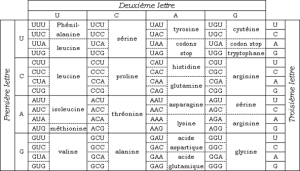
Les instructions dans un gène qui indiquent à la cellule comment fabriquer une protéine spécifique. A, C, G et T sont les «lettres» du code ADN; ils représentent respectivement l'adénine (A), la cytosine (C), la guanine (G) et la thymine (T) qui composent les bases nucléotidiques de l'ADN. Le code génétique est un ensemble de règles de correspondance permettant au message génétique constitué de nucléotides et porté sur l'ARNm d'être traduit en acides aminés protéinogènes. Cette correspondance est présentée sous forme de tableaux associant chacun des 64 codons, ou triplets de quatre bases nucléiques possibles (43 = 64), avec l'un des 22 acides aminés (Tabl. 4).
Étapes de la traduction
Fondamental :
- Étape d'initiation de la traduction
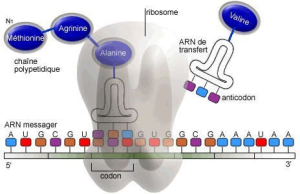
Elle correspond à la phase de reconnaissance du codon initial de la traduction (AUG : qui code pour la méthionine) de l'ARNm par la petite sous unité du ribosome et à l'assemblage d'un ribosome complet par accrochage de la grosse sous unité. Des facteurs protéiques interviennent dans cette étape: les facteurs d'initiation de la traduction. En effet, l'étape d'initiation se termine quand le codon initiateur de la traduction se lie à l'ARNt porteur de l'acide aminé méthionine) et que les deux sous unités du ribosome se lient entre elles.
- Étape d'élongation
C'est le déplacement du ribosome tout au long de l'ARNm et à l'accrochage séquentiel des acides aminés de la protéine en voie de biosynthèse.
Après la lecture du codon d'initiation, le ribosome fait le décalage d'un triplet de nucléotides pour passer au codon suivant et libérer un site pour un nouvel ARNt chargé et ainsi de suite.
La séquence de l'anticodon de l'ARNt se lie à un codon de l'ARNm, ainsi chaque ARNt porte un acide aminé particulier (il existe des ARNt glycine, ARNt valine etc ...selon la séquence de l'anticodon, les acides aminés chargés seront différents).
La grosse sous unité du ribosome, comporte trois sites de liaison pour les ARNt chargés de leur acide aminé (site P, site A et site E). Les acides aminés sont ajoutés les uns à la suite des autres par des liaisons peptidiques grâce à une activité peptidyl-transférase portée par le ribosome et ils sont détachés des ARNt. Ces derniers (sans acide aminé) quittent le ribosome au niveau du site E.
- Étape de terminaison
La terminaison de la traduction se fait grâce à un signal d'arrêt de la traduction qui est codé dans l'ARNm par un codon STOP (UAG, UGA ou UAA). Ces derniers sont reconnus par les facteurs de terminaison RF 1, RF 2 et RF 3 (RF pour Releasing Factor), ainsi la translocation du ribosome s'arrête, la chaine peptidique synthétisée est libérée et les deux sous unités du ribosome se séparent.
Maturation des protéines (Modifications post-traductionnelles)
La synthèse des protéines se produit au cours d'un processus appelé «traduction». Les modifications post-traductionnelles des protéines, étant l'une des dernières étapes de la biosynthèse des protéines, fait référence aux changements chimiques réversibles ou irréversibles que les protéines peuvent subir après la traduction, ce qui les rend matures pouvant remplir leur fonction au sein de l'organisme. En d'autres termes, les modifications sont des modifications chimiques d'une chaîne polypeptidique qui se produisent après que l'ADN a été transcrit en ARN et traduit en protéine dans le Réticulum endoplasmique et l'appareil de Golgi. . Ces changements chimiques se produisent lorsque des liaisons peptidiques sont coupées par des enzymes, ou lorsque des groupes chimiques spécifiques sont ajoutés aux lipides, aux glucides, voire même aux protéines entières ou aux chaînes latérales d'acides aminés. Les changements chimiques sur une chaîne de protéines après sa fabrication naturelle ajoutent de nouvelles structures et caractéristiques aux acides aminés, ce qui rend les protéines plus variées dans leurs structures et leurs fonctions.
Ces modifications des protéines ont pour rôle :
La régulation de leur activité.
Leur reconnaissance par d'autres molécules.
Leur fixation sur une membrane.
Leur implication dans les voies de signalisation.
Leur ciblage vers un compartiment cellulaire.
Les modifications post-traductionnelles misent en jeu différentes réactions enzymatiques et chimique, nous citons : le clivage des précurseurs polypeptidique, l'addition d'un groupe fonctionnel, l'addition de groupes peptidiques ou de protéines et les modifications chimiques des acides aminés.
a. Le clivage des précurseurs polypeptidique: correspond au clivage protéique par une protéase d'un lien peptidique, aboutissant à un changement structural de la protéine finale. Exemple : la réaction du clivage qui permet la transformation de la pro-insuline en insuline.
b. L'addition d'un groupe fonctionnel: les protéines sont modifiées par l'ajout es groupes fonctionnels, nous énumérerons quelques exemple :
- la prénylation, est la liaison d'un groupe isoprénoïde, appelée aussi terpénoïde.
- la glycosylation, coresspond à l'addition d'un groupe glycosyl sur un résidu asparagine, hydroxylysine, sérine, ou thréonine, produisant ainsi une glycoprotéine.
- la phosphorylation, qui est l'addition d'un groupe phosphate, généralement sur une sérine, tyrosine, thréonine.
c. l'addition de groupes peptidiques ou de protéines : l'ubiquitination c'est la réaction la plus courante, au cours de laquelle se déroule la formation d'une liaison covalente entre l'ubiquitine et une ou plusieurs lysines acceptrices de la protéine substrat.
d. les modifications chimiques des acides aminés : par exemple, la déamidation conduisant à la conversion de glutamine en acide glutamique ou de l'asparagine en acide aspartique.
Régulation de l'expression des gènes
La fonction cellulaire est influencée par l'environnement cellulaire. L'adaptation à des environnements spécifiques est obtenue en régulant l'expression de gènes codant pour les enzymes et les protéines nécessaires à la survie dans un environnement particulier.
Les facteurs qui influencent l'expression des gènes comprennent les nutriments, la température, la lumière, les toxines, les métaux, les produits chimiques et les signaux provenant d'autres cellules. Des dysfonctionnements dans la régulation de l'expression génique peuvent provoquer divers troubles et maladies chez l'homme.
Structure chromatinienne des gènes actifs
La structure de la chromatine joue un rôle important dans le contrôle de l'expression et de la réplication des gènes. La compaction de l'ADN dans les nucléosomes forme une structure «fermée» qui n'est pas très accessible aux enzymes qui affectent la transcription de l'ADN. Dans une structure nucléosomique «ouverte», l'ADN est plus accessible aux facteurs de transcription.
Lors de la transcription, certains agents activateurs et répresseurs interagissent avec les ARN polymérases pour modifier la structure de la chromatine et moduler l'activité des gènes. Les activateurs peuvent aider à perturber la structure du nucléosome et ainsi stimuler l'assemblage de l'ARN polymérase et des facteurs de transcription au niveau du promoteur.
a. La composition de la chromatine
La chromatine contient près de deux fois autant de protéines que d'ADN ; les principales protéines de la chromatine sont les histones, en outre, la chromatine contient une masse à peu près équivalente d'une grande variété de protéines non histones.
Les histones : petites protéines très riches en acides aminés basiques (arginine et lysine) qui favorisent la liaison aux charges négatives de la molécule d'ADN. il existe cinq types principaux d'histones, notées H1, H2A, H2B, H3, H4, formant un octamère d'histones constituant un cœur protéique en forme de disque (voir le cours de réplication).
Les protéines non histones : elles sont représentées par certaines protéines situées dans le noyau cellulaire mais non liées à l'ADN, nous citons par exemple: les topoisomérases, certaines ligases (E3-ligases), kinases nucléaires (MAP kinases) et cohésine....etc.
Ces facteurs protéiques assurent le bon déroulement des mécanismes vitaux pour la cellule : la transcription, la régulation de l'expression génique et la réplication.
b. La structure de chromatine
La chromatine structuralement est divisée en 2 parties:
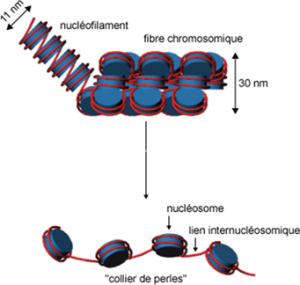
L'euchromatine : constitue la plus grande partie de la chromatine. Elle apparait décondensée pendant l'interphase et sous forme d'une structure en « collier de perles», chaque perle constitue une particule cœur de nucléosome (fig. 44).
L'hétérochromatine : elle un aspect dense foncée et condensée, localisée principalement en périphérie du noyau et du nucléole, ainsi elle possède une structure qui ne change pas d'état de condensation au cours du cycle cellulaire.
L'hétérochromatine à son tour est subdivisée en :
- l'hétérochromatine constitutive qui contient peu de gènes, formée principalement de séquences répétées et dont les plus grandes régions sont situées à proximité des centromères et des télomères.
- l'hétérochromatine facultative qui contient des régions codantes pouvant adopter les caractéristiques structurale et fonctionnelle de l'hétérochromatine, comme le chromosome X inactif chez la femme.
Régulation de l'expression des gènes chez les eucaryotes
L'information génétique d'une cellule eucaryote mille fois supérieure à celle d'une cellule procaryote. Les choses sont encore compliquées par le nombre de types de cellules et le fait que chaque type de cellule doit exprimer un sous-ensemble particulier de gènes à différents moments du développement d'un organisme.
Ils existent plusieurs mécanisme dont les eucaryotes régulent l'expression génique seront élucidées: la régulation transcriptionnelle et le traitement alternatif de l'ARN.
Régulation transcriptionnelle et post-transcriptionnelle
a. Au niveau transcriptionnel
- Grâce à la compaction chromosomique, les régions de chacun des différents chromosomes sont compactées sous forme d'hétérochromatine ou d'euchromatine. Dans l'hétérochromatine, l'ADN est très étroitement condensé et rendu inaccessible à la machinerie transcriptionnelle, par conséquent l'hétérochromatine devient inactive. Par contre, dans l'euchromatine, l'ADN n'est pas aussi condensé et est accessible à la machinerie de transcription.
- Méthylation de l'ADN : elle porte sur le carbone en C5 de cytosine qui précède une guanine (CG). Une telle méthylation a pour conséquence un verrouillage de l'expression génique. En effet, une hypométhylation favorise l'expression, alors dans le cas inverse la méthylation empêche le gène de s'exprimer.
- Eléments Trans régulateurs : les protéines qui participent à la régulation de l'expression des gènes sont souvent appelées éléments à action trans qui interviennent pour activer ou pour inhiber la RNA polymérase II et par suite induire ou réprimer l'expression du gène à transcrire. Ces facteurs trans-régulateurs se lient au DNA (DNA binding proteins) dans la région du gène située en amont de la partie transcrite.
Les facteurs agissant en Trans ont de multiples domaines requis pour l'activité et peuvent inclure des domaines de liaison à l'ADN ; exemple : le domaine hélice-coude-hélice.
- Eléments Cis régulateurs : les éléments régulateurs sont des séquences d'ADN spécifiques (généralement inférieures à 20 nucléotides) qui sont reconnues et liées par les éléments agissant en Trans qui stimulent ou inhibent l'expression d'un gène particulier.
Il existe deux types principaux d'éléments agissant en cis: les promoteurs et les éléments régulateurs :
- Les promoteurs sont les sites où l'ARN polymérase et la vitesse ou l'efficacité d'utilisation du promoteur par l'ARN polymérase est affectée par les éléments régulateurs.
- Les éléments régulateurs sont des séquences d'ADN spécifiques qui sont reconnues et liées par les éléments agissant en trans qui stimulent ou inhibent l'expression d'un gène particulier.
b. Au niveau post-transcriptionnel
Plusieurs types de régulation d'expression génique pourront intervenir après la transcription de l'ARN, nous à titre d'exemple l'épissage alternatif qui stipule qu'un gène peut coder des protéines différentes.
Des sites d'épissage alternatifs sont utilisés pour générer des protéines similaires avec des fonctions spécifiques aux tissus appelées isoformes. De nombreuses hormones peptidiques existent sous forme d'isoformes telles que le gène de la calcitonine qui est épissé de manière
différentielle pour produire de la calcitonine dans la thyroïde et un peptide lié au gène de la calcitonine dans les neurones (fig. 46).
Régulation au niveau traduction
Ce type de régulation se déroule dans le cytoplasme des cellules à l'inverse de régulation transcriptionnel qui a lieu au niveau du noyau.
- Les miARN : des ARN non codants (21-25 nucléotides) contrôlent l'expression génique en s'appariant avec des ARN cibles portant une séquence homologue permettant la répression de la traduction de la protéine correspondante ou clivant l'ARNm cible au niveau du site de fixation du micro ARN.
- La régulation par le 5'UTR met en jeu à la fois des structures spécifiques et des protéines régulatrices sur des séquences située entre la coiffe et le codon de démarrage de traduction (iron responsive element) pour bloquer le balayage par la sous-unité 40S du ribosome (eucaryotes). Ce mécanisme est en particulier rencontré pour la régulation du gène de la ferritine.
Régulation au niveau post-traductionnel
La régulation post-traductionnelle réfère au contrôle de la quantité de protéines actives.